Spenderorgane sind Mangelware und zudem mit Risiken verbunden.
07.09.2023 - 17:47:10Menschliches Nierengewebe wächst in Schweineembryos heran. Forschungsgruppen arbeiten an alternativen. Zu einem vielversprechenden Weg gibt es jetzt Ergebnisse.
Wissenschaftlern ist es gelungen, in Embryos von Schweinen Nierengewebe mit überwiegend menschlichen Zellen heranwachsen zu lassen. Dazu schalteten sie in den Embryos zwei Gene aus, die wichtig für die Entwicklung von Nieren sind. In diese Organlücke konnte dann Nierengewebe aus menschlichen Stammzellen hineinwachsen. Auf solche Weise gezüchtete Organe könnten später einmal Spenderorgane werden. Die Gruppe um Liangxue Lai von den Guangzhou Institutes of Biomedicine and Health in Guangzhou (China) stellt ihre Vorgehensweise in der Fachzeitschrift «Cell Stem Cell» vor.
«Rattenorgane wurden in Mäusen und Mäuseorgane in Ratten produziert, aber frühere Versuche, menschliche Organe in Schweinen zu züchten, waren erfolglos», erklärte Lai. Das Problem ist dasselbe wie bei Organspenden, wenn Spender und Empfänger nicht gut zueinander passen: Dann wird das Organ vom Körper des Empfängers abgestoßen, weil das Immunsystem es als fremdes Gewebe erkennt und Abwehrmaßnahmen einleitet. Hinzu kommt, dass die Schweinezellen im Embryo sich besser behaupten können als die menschlichen und beide Zelltypen unterschiedliche Bedürfnisse für ihr Gedeihen haben.
Mit Hilfe der Genschere Crispr/Cas entfernten die Forschenden aus einem einzelligen Schweineembryo die Gene SIX1 und SALL1, die für die Entwicklung von Nieren notwendig sind. Dadurch entwickelte der Embryo keine Schweinenieren, es entstand eine Leerstelle oder Nische. Aus Nabelschnurblut gewonnene menschliche pluripotente Stammzellen, aus denen alle Arten von menschlichen Zellen hervorgehen können, wurden in den Embryo gespritzt. Sie konnten sich in der geschaffenen Nische weitgehend konkurrenzlos zu Nierengewebe entwickeln.
Menschliche Stammzellen speziell präpariert
Die menschlichen Stammzellen waren zuvor speziell präpariert worden. Zum einen führte ein gentechnischer Eingriff dazu, dass vermehrt die Gene MYCN und BCL2 aktiviert wurden. Beide Gene sorgen für eine bessere Überlebensfähigkeit der Zellen, im Falle von BCL2 durch eine Verhinderung des programmierten Zelltods (Apoptose). Zum anderen gaben die Forscher die Stammzellen in ein kürzlich entwickeltes Nährmedium (4CL), das die Überführung der Stammzellen in frühere Entwicklungsstadien bewirkt; sie ähneln dann frühen menschlichen embryonalen Zellen.
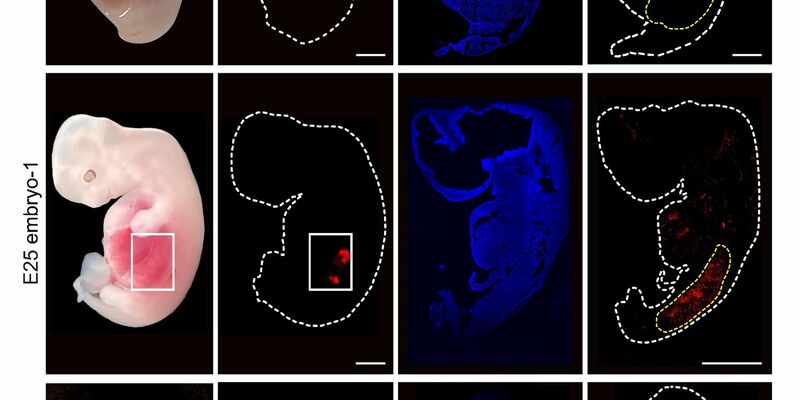
Die Schweineembryos pflanzten die Wissenschaftler in Säue ein, wo sie sich bis zum 25. oder 28. Tag entwickeln konnten. Es gab einige Embryonen, bei denen sich eine Niere aus überwiegend menschlichen Zellen im Vergleich zu nicht behandelten Schweineembryonen normal entwickelt hatte. Das Verfahren ist aber noch verbesserungsbedürftig: «Der Gesamtanteil degenerierender Schweinembryonen ist hoch, und es muss beurteilt werden, ob dies teilweise mit dem Chimärismus oder anderen Aspekten des Injektionsverfahrens zusammenhängt», schreiben die Studienautoren.
Auch die gut gewachsenen Nieren enthalten zudem noch zu mehr als einem Drittel Zellen von Schweinen, was bei einer Organverpflanzung beim menschlichen Organismus zu Abwehrreaktionen führen kann. «Da Organe nicht nur aus einer einzigen Zelllinie bestehen, müssten wir die Schweine wahrscheinlich auf viel komplexere Weise manipulieren, um ein Organ zu bekommen, in dem alles vom Menschen stammt», sagte Mitautor Miguel Esteban von den Guangzhou Institutes of Biomedicine and Health.
Nabelschnurblut als Grundlage der menschlichen Stammzellen
Medizinethiker Wolfram Henn vom Deutschen Ethikrat hebt bei seiner Einschätzung zur Studie positiv hervor, dass als Grundlage der menschlichen Stammzellen Nabelschnurblut verwendet wurde. Dadurch werde die Nutzung menschlicher Embryonen vermieden. Außerdem biete das Verfahren eine Perspektive dafür, dass künftig eigene Blutstammzellen eines Patienten, der auf ein Spenderorgan angewiesen ist, als Basis für die Züchtung des Organs verwendet werden könnten. Weil dann die eingesetzten Zellen vom Patienten selbst stammen würden, dürfte es in der Regel keine Abstoßungsreaktionen geben. Insgesamt beurteilt er das Vorgehen der Forscher als vernünftig und verantwortungsbewusst.
Auch im Hinblick auf den Tierschutz hält Henn das Verfahren für ethisch vertretbar: «Wir züchten Tiere, um sie zu essen, da ist es nicht verwerflich, Tiere zu züchten, um Menschenleben zu retten.» Für wichtig hält Henn vor allem, dass das deutsche Recht modernisiert wird, da das Embryonenschutzgesetz mittlerweile mehr als 30 Jahre alt sei. Viele der heute angewendeten Verfahren habe es damals noch nicht gegeben, so dass die gesetzliche Grundlage für eine Forschung, wie sie in der Studie beschrieben wurde, neu gefasst werden müsse, forderte der Medizinethiker.